导读: 本期的文献通译是一篇关于生物样品库的专业文章。 生物样品库对现代生物医学的发展, 尤其是生物标记物的开发和确认, 对于个体化医疗的推广, 以及对于我们所关注的液体活检领域的发展, 都起到了越来越多的支撑作用。 但是生物样品库也面临着瓶颈, 最显著的就是生物样品库种类繁多, 标准混乱。 本文阐述了建立生物样品库的过程, 它从方法学开始, 针对一个专一的癌症病种,通过文献、咨询、协商和统计分析, 明确提出了采集样品和数据的若干工具, 并参照地区、国家和国际的标准, 对新建的生物样品库的标准作出harmonisation, 就是协调标准以达共识。 生物样品库的规范化, 必然将其推向独立发展的学科和业务领域, 值得阳普这样的样品专家的关注和跟踪。
原文出处
British Journal of Cancer (2017) 117, 485-493
作者
M Adishesh1,2, A Fyson2, S B DeCruze1, J Kirwan1, ENITEC Consortium, H M J Werner3,4 and D K Hapangama*,1,2
作者信息
Liverpool Women’s Hospital NHS Foundation Trust, Crown Street, Liverpool L8 7SS, UK; Department of Women’s and Children’s Health, Institute of Translational Medicine, University of Liverpool, Liverpool Women’s Hospital, Crown Street, Liverpool L8 7SS, UK; 3Department of Obstetrics and Gynaecology, Haukeland University Hospital, Jonas Liesvei 70, 50503 Bergen, Norway and 4Department of Clinical Science, University of Bergen, Bergen 5021, Norway
摘要
背景:子宫内膜癌是最常见的妇科癌症,预计其发病率到2025年将上升50-100%,相关死亡率也将相应增加。生物学样本的收集、处理和储存过程中的是否一致会影响到科学数据的普遍性。本旨在协调与子宫内膜癌相关的生物样本以及临床数据的收集,并制定收集、处理和储存子宫内膜癌生物样本的标准操作程序。
方法:我们设计了通过三个共识轮次进行评估和修订的研究工具,以获得地方/区域、国家和欧洲的共识。修改的最终工具被传播给代表子宫内膜癌研究的所有利益相关者的小组(n = 40),以达成共识。
结果:最终的共识表明与最小的手术和患者数据收集工具的一致同意。另外还有其他标准工具的高度一致意见。
结论:我们在这里介绍了所有子宫内膜癌研究人员可以免费使用的工具的最终版本。我们认为,这些工具将促进子宫内膜癌研究的快速进展,无论是在未来的合作还是大规模的多中心研究中。
背景介绍
子宫内膜癌(EC)是发达国家女性生殖道最常见的癌症,是乳腺癌、肺癌和结肠直肠癌后女性第四大常见癌症(Ferlay等,2015)。在2014年,英国每天至少有6名妇女死于子宫内膜癌,同时有21名妇女被诊断患有子宫内膜癌。欧共体每年有9022例新发病例和2166例死亡病例(CRUK)。 EC的发病率迅速增加,预计到2025年将增加50-100%(Lindemann等,2010)。这种发病率的上升令人震惊,特别是由于死亡率相应上升(CRUK)。因此迫切需要更多地努力寻找新的预防,诊断,预后和治疗目标,以降低与欧共体相关的高死亡率和发病率。传统上,使用基于福尔马林固定石蜡包埋组织的免疫组织化学,仅允许同时研究有限数量的蛋白质。虽然其他细胞系和动物研究已被应用于欧共体研究, 但是这些很少提供体内人体环境的完美模拟。因此,收集广泛的不同患者标本(包括例如新鲜的冷冻组织,尿液,血液或唾液)的生物库在为临床相关科学发现提供有价值的患者材料方面起着至关重要的作用,也有助于快速翻译基础科学发现临床实践。
通过其特殊性质,存储在生物样本中的患者材料使研究EC的多个方面成为可能。随着基因组学,蛋白质组学,表观基因组学和代谢组学等新技术平台的出现,这些技术平台可以统一并同时应用于相同的患者样本,以获得最大限度的信息,这一点至关重要。预期这种全面的方法将大大减少新的基础科学发现以新的治疗方式接触患者所花费的时间,并允许患者捐赠的样品被充分利用。
生物样本库所产生的数据的内部和外部的有效性取决于其质量,这显然取决于严格标准在收集生物样本和患者特征方面的使用。与收集,处理,存储不同生物样本和伴随的表型和人口统计数据相关的变化使得极其难以推断或合并来自不同研究的数据(Tworoger和Hankinson,2006; Ransohoff和Gourlay,2010)。国家癌症研究所(NCI)认为缺乏质量标准和统一性是癌症研究的障碍(NCI最佳实践,2011年生物世界资源)。标本和数据收集中的不规则性和不相似性所引起的不可逆转的偏见得到许多人的认可,许多国际组织和机构正在努力克服这一点(Morente等人,2007年;国际生物与环境储存学会,2008年; Yuille等,2008; Vaught and Lockhart,2012)。
鼓励优化可用于癌症研究的资源的生物样品库NCI最佳实践指南(NCI Best Practices for Biospecimen Resources,2011年,2016年)广泛提及与捐赠者或样本收集/处理相关的预分析变量的有限列表。从而有效提高了涉及生物样本的研究的整体意识和质量。
虽然这是一个重要的开始,但许多参数和变量,包括生物样本和临床数据的选择,都是癌症型特异性的。因此,普遍的生物网路化标准不一定适用于每种癌症类型,并且应适应于每种特定疾病。癌症基因组图谱(Kandoth et al,2013)强调了癌症特异性协调生物样品库业标准的重要性,该基因组图谱现在包含超过532个具有RNA测序,拷贝数变异,蛋白质组学,突变和微阵列数据的ECO样品。然而,这些样本和数据集中大部分的临床数据非常有限,严重影响了研究人员绘制临床适用信息的能力。
因此,EC特异性标准化采集具有独特和相关的临床数据集的生物样本是改善未来EC研究的根本未满足的需求。我们相信,这将有助于未来对EC的大规模国际合作研究,这可能导致改进的生物标志物和靶标治疗发现。子宫内膜异位症 - 世界子宫内膜异位症研究基金会子宫内膜异位症和生物样品库协调项目和卵巢癌研究计划(Wiegand et al,2010; Heravi-Moussavi et al,2012; Fassbender et al, 2014; Rahmioglu等,2014; Vitonis等,2014)。
有了这个背景,我们开始了研究(Harmanization of biobAnking Standards in Endometrial caNcer research - HASTEN),以达成EC研究人员的共识;规范所有相关生物样本的收集,处理和储存;以及通过与患者,外科医生/医师/病理学家和生物工程人员的共同努力进行EC研究的随附临床数据。我们旨在制定标准:标准操作程序工具,最小和标准数据集将定期更新,并普遍适用于EC的未来研究人员。
材料和方法
流程图总结了用于设计HASTEN中最终工具的方法(图1)。我们使用修改后的德尔福系统来分析和确认最终的共识。
我们的生成初始工具的过程起始于文献检索。我们使用关键词“子宫内膜癌”,“危险因素”,“介绍年龄”,“平等”,“绝经状态”,“二甲双胍”,“孕激素或曼月乐”,“激素替代疗法” '多囊卵巢综合征','他莫昔芬','肠癌','结肠直肠癌','乳腺癌','糖尿病','高血压','种族','人体测评','吸烟' “子宫内膜”,“血液或血浆或血清”,“唾液”,“尿”,“子宫内膜液”,“腹膜液”,“生物样品库最佳实践”组织病理学标志物,“结果” ',“组织,血液和体液的实验室处理程序”,“生物分类标准”,“收集组织、液体、血液、唾液、尿液的SOP”,用以上的关键词搜索了Scopus,Discover和PubMed数据库。文献搜索仅限于过去10年发表的研究。在初步搜索中确定的3464篇论文中,根据以下纳入标准,选择了413篇文章进行进一步的详细审查:
(1)调查上述因素如何影响个人发展EC风险的论文。
(2)提出标准操作程序(SOP)或收集,储存和加工不同组织或液体的最佳做法的出版物。
(3)只有英文的论文。
(4)可通过所有可用资源向作者提供论文(例如,利物浦妇女医院(LWH),利物浦大学,英国医学协会或皇家妇产科学院的在线资源或图书馆设施。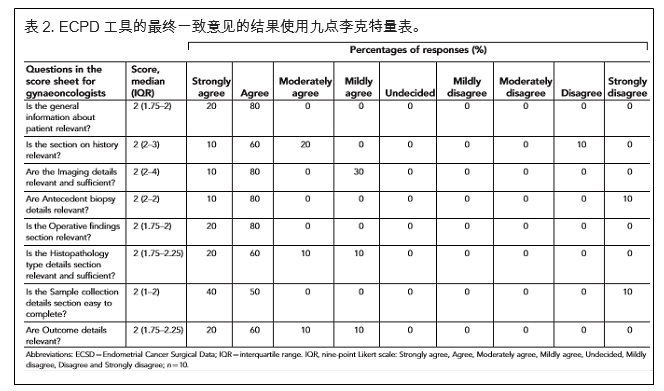
我们进一步对这些选定论文中引用的相关手稿进行手动搜索,并从大型生物解毒剂中进行相关指导。
工具的进一步开发
首次当地咨询。利物浦的当地团队由四名外科妇科肿瘤学小组成员组成,四名麦克米伦临床癌症护士专家,两名对EC研究感兴趣的临床学者,两名病理学家,两名生物工作人员和一名医学生,开发出三种形式患者数据收集工具,手术数据收集工具,生物样本表格)和标准手术程序。这些形式和SOP基于:(a)文献搜索中收集的信息; (b)由
考虑到LWH /利物浦大学生物库中已经使用的形式,用于收集EC研究中的生物样本和数据。利物浦妇女医院是妇科癌症的高等转诊区域癌症中心,是柴郡和默西塞德战略临床网络的一部分,为240万人口提供服务。默西塞德郡和柴郡癌症网络的EC年龄标准化发病率为18.3 / 10万女性成员(NCIN,2013; Gynae Clinical Network Constitution,2014-2015)。 (c)由国立卫生研究院,人子宫内膜组织和DNA银行开发的用于收集,运输和储存子宫内膜组织和进行子宫内膜活检或子宫切除术的非恶性指征的女性血液样本的标准操作程序(Sheldon等,2011)。 (d)英国生物库公布的收集尿液和血液样本的样品处理和储存方案(Elliott等,2008)。英国生物样品库是维康信托,医学研究理事会,卫生部,苏格兰政府和西北地区发展局成立的国家和国际重要卫生资源。
其主要目的是改善癌症,心脏病,中风,糖尿病,关节炎,骨质疏松症,痴呆等许多疾病的预防,诊断和治疗。
二次区域/国家磋商。上述三种形式的修改版本和上述SOP在联合王国参与欧共体研究的三个区域和八个国家研究中心之间传播,形式修订整合了其反馈,结果是两种不同的工具,一种是最小的和一种开发了标准工具。这种务实和包容性的方法为考虑可用资源收集最小或理想的“标准”数据集提供了指导。
第三次欧洲咨询。然后将修改后的表格分发给所有坚持欧洲子宫内膜癌个性化治疗网络(ENITEC)的研究人员,并根据收到的反馈进一步修订。修订的工具在2016年6月的年度ENITEC面对面会议上提出,最小形式得到所有47名与会者的一致通过。对标准工具进行了一些进一步修改,并作了相应修订,修订后的表格重新填补了所有参加第1-3次磋商的情况,得到最后的批准。
达成共识。 共识一代修改后的Delphi系统被用于对最终的修改工具产生共识。为此,将这些表格传播给代表所有前几轮所有利益相关者的一组选定小组成员,包括患者,
妇科肿瘤学家,研究人员,病理学家和生物工作人员,从咨询参与者(n = 40)随机选择使用记录他们的协议的评分表评估和评分工具。
统计分析。使用修改的德尔菲技术对共识进行了量化,我们已经报告了中位数为四分位数范围,并且还有Likert量表的每个类别的百分比。使用了九分李克特量表,除了患者数据工具,其量表减少到五点,以减少患者的复杂性。
结果
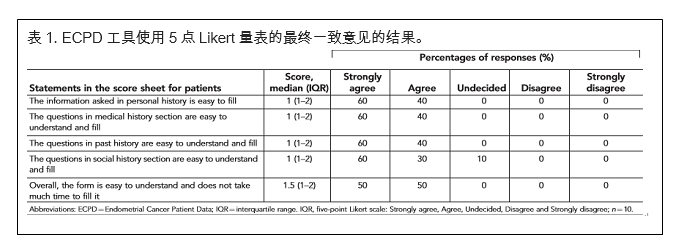
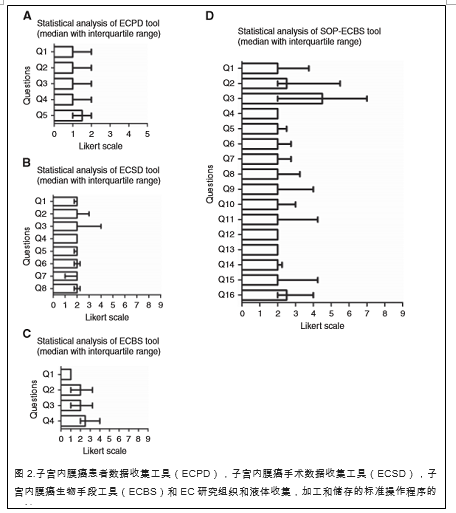
本研究的最终工具是ECPD收集工具。我们设计了一种耐心友好的数据收集工具(EC患者数据(ECPD))来捕获与EC研究直接相关的许多重要人口统计学变量,只能由患者自己准确回忆。例如,现有的文献表明420 kg与EC增加风险独立相关的成人体重增加(Friedenreich et al。,2007)和这种信息不可能直接从患者身上获得。 EC的许多其他危险因素,如介绍年龄,绝经后状态,多囊性卵巢疾病(Fearnley等,2010),无效性(Schonfeld等,2013),月经初潮(Gong等,2015),家庭遗传性疾病综合征性癌症的历史(Boilesen等人,2008),过去的疾病综合征相关癌症病史,糖尿病等医学病症(Friberg等,2007),先前使用他莫昔芬(Bergman等,2000),激素替代疗法使用(Beral等人,2005年)和运动习惯已被纳入该工具。目前还有一些其他因素与目前的EC(如Lindemann等人,2008)没有任何联系,因为他们在今后的研究中肯定了这一点。表1和图2说明了最后一轮协商一致的结果。
ECPD中每个问题的得分使用Likert量表获得,Likert量表评估可接受性和可用性(n = 10)。在小组成员中,只有2%在社会历史部分的问题清晰度方面未定,总共98%的患者同意该工具易于使用。
ECSD收集工具。 EC手术数据(ECSD)工具包括突出的人口统计学,组织学和术前/术后特征。包括人体特征如体重指数(BMI)。选择身体质量指数代替腰臀比或腰围,因为其普遍使用和重现性。尽管所有人体测量(BMI,腰臀比,腰围和臀围周围)都被发现与EC风险增加密切相关(Friedenreich等,2007),腰臀比或腰围的准确数据需要额外的努力使用医疗团队相同的参考点,因此准确的数据收集不可能普遍可行。在最近的一项研究(Painter等,2016)中,BMI被发现是一个因素,与EC与腰臀比相关。术前成像细节有助于评估局部扩散和排除远处转移。子宫内膜活检和最终组织学结果之间的差异已被证明与较差的生存结果相关(Werner等,2013);因此,术前活检结果很重要。与结果相关时,手术后的分期细节,包括手术结果和最终组织病理学细节是重要的。免疫组织化学生物标志物可用于区分卵巢癌,子宫颈癌或其他恶性肿瘤,但重要的是与临床预后相关的预后生物标志物(Li等,2013; Kamal等,2016)。以标准方式与生物样本一起收集的信息自然会增加生成数据的内部和外部有效性。应定期更新患者资料,包括随访和准确记录死亡原因,直至完成标准随访期(3年(至少)或5年,视当地实践而定)。表格分为三个部分:
(1)手术资料:收集样本时完成。
(2)组织病理学细节:最终分期治疗后完成。
(3)结果数据:在随访期间记录,最后在随访结束时记录。

最终共识的结果如表2和图2所示,其中我们用四分位数范围计算了中位数。所有小组成员的小组成员之间达成了高度的一致意见,但一些答复者认为有关历史,先前活检细节和样本收集细节的部分不相关。总体来说,96.25%的小组成员同意该工具的不同方面(补充图S1)。
|
|
用于EC研究的组织和液体的收集,加工和储存的标准操作程序。 EC研究中研究了不同组织类型(子宫和宫外)和体液类型。这些生物样本的常规研究可能涉及使用蛋白质组学,基因组学和代谢组学等多种技术提取待评估的蛋白质,RNA和DNA。最终的SOP设计合并了许多可用的单独的详细方法方案(例如,用于离心,过滤,添加防腐剂以及储存温度)。从生物库获得这些信息将使科学家能够准确地解读其数据,例如检查血液,组织,子宫内膜液或抽吸物等样品的代谢特征,并自信地检测疾病特异性变化,特别是在多中心研究中(Assfalg等人,2008; Bernini等人,2009)。检查激素的研究与子宫内膜有重要关系,除了传统的血液样本之外,还有一些研究人员研究了非侵入性标本,包括唾液和尿液(Shirtcliff等,2001)。非侵入性测试对临床研究特别有兴趣,未来工作预计将更多地集中在他们身上。
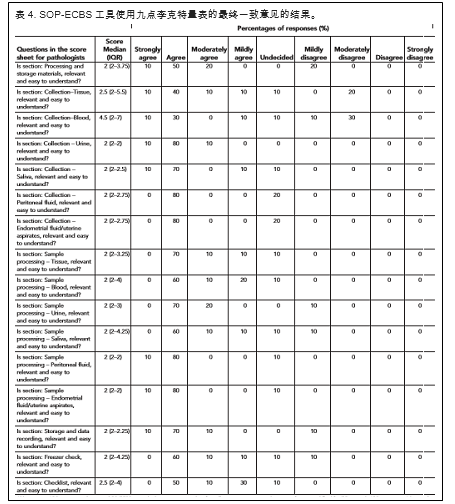
关于用于EC研究(SOP-ECBS)的组织和液体的收集,处理和储存的标准操作程序的最终一致意见的结果细节如表4和图2所示。关于用户的一般性协议友好和工具的相关性。少数小组成员回答说,为了清楚起见,可以进一步修改组织和血液收集细节。总体上,83.75%的小组成员同意,8.75%未定,7.5%不同意这一工具的不同部分。
讨论
我们已经开发了以证据为基础的标准数据收集表格ECPD,ECSD(最小),ECSD(标准)和SOP-ECBS,包括所有利益相关者在EC癌症生物样品库中的参与和批准。最终的工具被一个大型的多学科评审小组批准,达成一致后(见补充图S1),它们作为补充信息公布在这个开放存取手稿中。因此,他们将免费向国际上所有的欧盟研究人员提供。这些工具提供了一种减少收集数据中的混杂因素并促进更大型多中心研究的方法。
我们选择要收集的确切信息是基于对最佳现有证据的批判性评估。没有公开证据的地方,考虑了专家意见和较大生物库的SOPs的咨询。处理血液的离心速度就是这样一个例子。
我们使用了一种修改后的德尔菲技术,该标准技术具有多项改进,包括多轮反馈,允许相同的小组成员重新评估或重新考虑初步判断,参与者匿名性,受控反馈和统计分析以解释轮次之间的数据。以前已经使用了与原始德尔福系统相似的变化,例如限制专家对专家组的原始问题和变更的响应能力以及改变终点的能力(Thompson,2009)。
对于我们的研究目的,反复使用同质小组是不合理的,原因如下。我们的努力是为不同的终点产生单独的形式,例如患者数据收集,手术数据收集,组织处理信息和标准手术程序。这些明显需要不同背景的小组成员,具有不同的专业领域,因此我们的小组成员不是一个同质的组织。
与经典技术的主要偏差是咨询轮次数和终点数。我们的前两轮是描述性的,以产生不同专家组的意见和想法。我们包括他们的反馈,以产生最终的表格和SOP。在最后一轮的协商一致意见中,我们向每个小组成员分发了一张表格,并附上表格,评估他们与最终工具的协议。我们的最后一个小组包括所有以前小组参与的利益相关者。通过对从第三轮和最后一轮获得的数据的统计分析观察到的高比例的协议排除了进一步的共识轮回的需要。
更详细的是,标准化的手术数据收集将可以全面评估外科表型数据与治疗结果之间的关系,我们强烈建议使用标准而不是最小的ECSD工具。但是,如果无法保证大量数据或样本的收集或质量,则应采用最小集合。我们计划通过反馈和未来文献综述获取的信息,定期更新这些工具,最初是每年5年,之后5年。在我们的举措范围内的未来考虑包括建立一个国际资助的基于网络的中央数据库系统,允许自愿将信息存储在全球范围内的欧洲研究组织研究人员收集的所有生物样本信息中。我们认为,这种方法可以降低各个单位的成本和时间,同时增加生成的数据的可信度,并为更新的协作提供一个透明的通用平台。
“分子病理流行病学”(MPE)整合了病理学和流行病学,以了解影响癌症发生,进展和治疗反应的外源性和内源性因素之间的相互关系。它是癌症研究中不断发展的领域(Ogino和Stampfer,2010)。还开发了统计学方法来考虑分子病理学和流行病学,以确保具有高临床影响的新发现。然而,与传统的分子生物学研究(Hughes等人,2012; Campbell等,2017)相似的类似挑战,包括选择和回忆偏倚,测量误差和错误分类,这些高度影响的MPE研究的产生受到阻碍。组织检索率和样本量的变异性导致随机和非随机选择偏倚,导致效应估计与宽置信区间和出版偏倚的巨大差异(Ogino等,2011,2016)。 EC生物库使用我们的工具将提供一种手段,简化从表型良好的患者中收集大量标准化的质量保证材料。这将反过来促进充分动力的研究,提供高临床影响,同时也促进在可接受的时间范围内可达到的高质量研究。